Бутамират является противокашлевым средством центрального действия.
Бутамирата цитрат обладает неспецифическими антихолинергическим и бронхоспазмолитическим эффектами.
Подавляет кашель, обладая прямым влиянием па кашлевой центр. Оказывает бронходилатирующий эффект (расширяет бронхи). Способствует облегчению дыхания, улучшая показатели спирометрии (снижает сопротивление дыхательных путей) и оксигенации крови (насыщает кровь кислородом).
Фармакотерапевтическая группа: противокашлевое средство с центральным механизмом действия.
МНН: бутамират.
Показания к применению: Бутамират-Фармстандарт показан для симптоматического лечения сухого кашля различной этиологии у взрослых и детей старше 3 лет.
Отпускают без рецепта.

|
ОБЩАЯ ХАРАКТЕРИСТИКА ЛЕКАРСТВЕННОГО ПРЕПАРАТА
1. НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
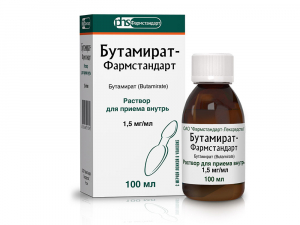
Бутамират-Фармстандарт, 1,5 мг/мл, раствор для приема внутрь.
2. КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Действующее вещество: бутамират
1 мл раствора содержит 1,5 мг бутамирата (в виде цитрата).
Вспомогательные вещества, наличие которых надо учитывать в составе лекарственного препарата: сорбитол (сорбитола раствор 70 % некристаллизующийся), глицерол (глицерин), натрия сахаринат, натрия гидроксид (см. раздел 4.4).
Полный перечень вспомогательных веществ приведен в разделе 6.1.
3. ЛЕКАРСТВЕННАЯ ФОРМА
Раствор для приема внутрь.
Прозрачная, бесцветная или с желтоватым, или коричневато-желтым оттенком вязкая жидкость с запахом корицы.
4. КЛИНИЧЕСКИЕ ДАННЫЕ
4.1 Показания к применению
Бутамират-Фармстандарт показан для симптоматического лечения сухого кашля различной этиологии у взрослых и детей старше 3 лет.
4.2 Режим дозирования и способ применения
Режим дозирования
Внутрь.
Взрослые: по 15 мл 4 раза в сутки.
Максимальная суточная доза - 60 мл (90 мг).
Не превышайте рекомендованную дозу!
Максимальная длительность применения препарата без консультации с врачом: 7 дней.
Дети
Дети старше 12 лет: по 15 мл 3 раза в сутки.
Максимальная суточная доза - 45 мл (67,5 мг).
Дети в возрасте от 6 до 12 лет: по 10 мл 3 раза в сутки.
Максимальная суточная доза - 30 мл (45 мг).
Детям от 3 до 6 лет: по 5 мл 3 раза в сутки.
Максимальная суточная доза - 15 мл (22,5 мг).
Препарат Бутамират-Фармстандарт в данной лскарственной форме противопоказан детям младше 3-х лет.
Способ применения
Препарат принимают с пищей. Используйте прилагаемую мерную ложку (см. раздел 6.6). При усугублении симптомов или отсутствии улучшения состояния после 7 дней лечения, а также при повышении температуры, сыпи или стойкой головной боли, следует обратиться к врачу для проведения дальнейшего обследования.
4.3 Противопоказания
• Гиперчувствительность к действующему веществу или к любому из вспомогательных веществ, перечисленных в разделе 6.1;
• детский возраст до 3 лет;
• беременность (см. раздел 4.6);
• период грудного вскармливания (см. раздел 4.6);
• дефицит сахаразы/изомальтазы, непереносимость фруктозы, глюкозо-галактозная мальабсорбция;
• одновременный прием отхаркивающих препаратов.
4.4 Особые указания и меры предосторожности
B связи с тем, что бутамират подавляет кашлевой рефлекс, следует избегать одновременного применения отхаркивающих средств во избежание скопления мокроты в дыхательных путях с риском развития бронхоспазма и инфскции дыхательных путей.
Вспомогательные вещества
Раствор для приема внутрь содержит в качестве подсластителей сахаринат и сорбитол (405 мг в одном мл), поэтому может назначаться больным с сахарным диабетом. Препарат содержит сорбитол - если у Вас непереносимость некоторых сахаров, обратитесь к лечащему врачу перед приемом данного лекарственного препарата. Сорбитол является источником фруктозы. Пациентам с наследственной непереносимостью фруктозы не следует принимать данный лекарственный препарат. Сорбитол может вызывать дискомфорт в желудочно-кишечном тракте и оказывать легкое слабительное действие.
Препарат содержит глицерол который может вызывать головную боль, расстройство желудка и диарею (понос).
Препарат содержит менее 1 ммоль (1,23 мг) натрия в дозе, т.е. практически «не содержит натрия».
4.5 Взаимодействия с другими лекарственными препаратами и другие формы взаимодействия
Клинически значимого взаимодействия препарата с лекарственными препаратами других групп не выявлено.
Какие-либо лекарственные взаимодействия для бутамирата не описаны.
B связи с тем, что бутамират подавляет кашлевой рефлекс, следует избегать одновременного применения отхаркивающих средств во избежание скопления мокроты в дыхательных путях с риском развития бронхоспазма и инфекции дыхательных путей (см. раздел 4.4.1).
4.6 Фертильность, беременность и лактация
Беременность
Данные о применении бутамирата у беременных женщин отсутствуют.
Исследования репродуктивной токсичности на животных не свидетельствуют о наличии прямых или непрямых вредных эффектов (см. раздел 5.3).
В качестве предупредительной меры предпочтительно не применять препарат Бутамират-Фармстандарт во время беременности.
Лактация
Сведения о проникновении действующего вещества препарата (его метаболитов) в грудное молоко человека отсутствуют.
В качестве предупредительной меры предпочтительно не применять препарат Бутамират-Фармстандарт во время грудного вскармливания.
Фертильность
Данные о влиянии препарата на фертильность человека отсутствуют.
4.7 Влияние на способность управлять транспортными средствами и работать с механизмами
Бутамират-Фармстандарт оказывает умеренное влияние на способность управлять транспортными средствами и работать с механизмами.
Бутамират в редких случаях может вызывать сонливость. В случае появления сонливости следует воздержаться от управления транспортными средствами и работы с механизмами.
4.8 Нежелательные реакции
Для определения частоты возникновения побочных эффектов препарата применяют следующую классификацию: очень часто (≥ 1/10); часто (≥ 1/100 и < 1/10); нечасто (≥ 1/1000 и < 1/100); редко (≥ 1/10000 и < 1/1000); очень редко (< 1/10000); частота неизвестна (не может быть установлена на основании имеющихся данных).
Нарушения со стороны нервной системы:
Редко: сонливость.
Желудочно-кишечные нарушения:
Редко: тошнота, диарея.
Нарушения со стороны кожи и подкожных тканей:
Редко: крапивница, возможно развитие аллергических реакций.
Сообщение о подозреваемых нежелательных реакциях
Важно сообщать о подозреваемых нежелательных реакциях после регистрации лекарственного препарата с целью обеспечения непрерывного мониторинга соотношения "польза - риск" лекарственного препарата. Медицинским работникам рекомендуется сообщать о любых подозреваемых нежелательных реакциях лекарственного препарата через национальные системы сообщения о нежелательных реакциях государств – членов Евразийского экономического союза.
Россия
Уполномоченный орган (уполномоченная организация) государства - члена Евразийского экономического союза: Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор)
Адрес: 109074, Москва, Славянская площадь, д. 4, стр. 1
Тел. : +7 (495) 698-45-38 , +7 (499) 578-02-30
Факс: +7 (495) 698-15-73
Электронная почта: pharm@roszdravnadzor.ru
Сайт в информационно-телекоммуникационной сети «Интернет»: www.roszdravnadzor.ru
4.9 Передозировка
Симптомы: признаки острого отравления при попадании внутрь: сонливость, тошнота, рвота, диарея, головокружение и снижение артериального давления. Пострадавшему следует немедленно обратиться к врачу.
Лечение: симптоматическое. Меры помощи при передозировке включают: удаление препарата из желудка и кишечника (промывание желудка, искусственная рвота, клизма,применение кишечных адсорбентов - активированного угля), поддержание жизненно-важных функций организма. Специфического антидота нет.
5. ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
5.1 Фармакодинамические свойства
Фармакотерапевтическая группа: Противокашлевое средство центрального действия
Код АTX: R05DB13
Механизм действия и фармакодинамические эффекты
Бутамират является противокашлевым средством центрального действия. Однако точный механизм действия препарата не известен. Бутамирата цитрат обладает неспецифическими антихолинергическим и бронхоспазмолитическим эффектами.
Подавляет кашель, обладая прямым влиянием па кашлевой центр. Оказывает бронходилатирующий эффект (расширяет бронхи). Способствует облегчению дыхания, улучшая показатели спирометрии (снижает сопротивление дыхательных путей) и оксигенации крови (насыщает кровь кислородом). В терапевтических дозах препарат хорошо переносится. Бутамират в форме раствора для приема внутрь оказывает успокаивающее действие на раздраженное горло благодаря увлажняющим свойствам глицерола.
5.2 Фармакокинетические свойства
Фармакокинетика
Абсорбция
Бутамират быстро и полностью всасывается и гидролизуется в 2-фенилмасляную кислоту и диэтиламиноэтоксиэтанол. Влияние одновременного приёма пищи на процессы не изучалось. Содержание 2-фенилмасляной кислоты и диэтиламиноэтоксиэтанола в плазме полностью пропорционально в диапазоне доз 22,5 мг - 90 мг.
Измеряемые концентрации бутамирата обнаруживаются в крови через 5-10 минут после приема доз 22,5 мг, 45 мг, 67,5 мг и 90 мг. Максимальная концентрация в плазме достигается через 1 час после приема всех 4 доз, а средняя максимальная концентрация составляет 16,1 нг/мл при приеме дозы 90 мг.
Средняя максимальная концентрация 2-фенилмасляной кислоты достигается в течение 1,5 часов; максимальная экспозиция отмечается после применения 90 мг (3052 нг/мл).
Средняя максимальная концентрация диэтиламиноэтоксиэтанола достигается через 0,67 ч; максимальная экспозиция также отмечается после приема 90 мг (160 нг/мл).
Распределение
Бутамират имеет объем распределения между 81 - 112 л (с поправкой на массу тела в кг), а также высокую степень связывания с белками плазмы. 2-фенилмасляная кислота имеет высокую степень связывания с белками плазмы в диапазоне дозе 22,5 - 90 мг, имея среднее значение 89,3% - 91,6%. Диэтиламиноэтоксиэтанол в некоторой степени связывается с белками плазмы крови, средние значения варьируют от 28,8% до 45,7%. Нет данных о проникновении бутамирата через плацентарный барьер и его выделении с грудным молоком.
Биотрансформация
Гидролиз бутамирата происходит быстро, концентрации метаболитов обнаруживаются через 5 минут. На основании данных исследований, считается, что эти метаболиты также обладают противокашлевой активностью, однако нет клинических данных о метаболизме диэтиламиноэтоксиэтанола. 2-фенилмасляная кислота подвергается дальнейшему частичному метаболизму гидроксилированием в пара-положении.
Элиминация
Через 24 часа после приема препарата основные метаболиты (77%) состоят из конъюгированной 2-фенилмасялной кислоты и парагидрокси-2-фенилмасялной кислоты.
Выведение 2-фенилмасляной кислоты, диэтиламиноэтоксиэтанола и п-гидрокси-2- фенилмасялной кислоты осуществляется преимущественно с мочой.
Уровень конъюгата 2-фенилмасляной кислоты в моче значительно превышает сго уровень в плазме. Бутамират определястся в моче в течение 48 часов после приема препарата внутрь.
Количество бутамирата, выделяющегося в мочу в течение 96 часов, соответствует 0,02, 0,02, 0,03 и 0,03% при дозах препарата 22,5 мг, 45 мг, 67,5 мг и 90 мг. В большем количестве выводятся метаболиты бутамирата. Период полувыведения бутамирата - 1,48-1,93 часа, 2-фенилмасляной кислоты - 23,26-24,42 часа, диэтиламиноэтоксиэтанола - 2,72-2,90 часов.
Особые группы пациентов
Отсутствуют данные об изменении фармакокинетики препарата у пациентов с нарушением функции печени или почек.
5.3 Данные доклинической безопасности
В доклинических данных, полученных по результатам стандартных исследований фармакологической безопасности, токсичности при многократном введении, генотоксичности и репродуктивной и онтогенетической токсичности, особый вред для человека не выявлен.
Исследования канцерогенного потенциала бутамирата не проводились.
6. ФАРМАЦЕВТИЧЕСКИЕ СВОЙСТВА
6.1 Перечень вспомогательных веществ
Сорбитол (сорбитола раствор 70 % некристаллизующийся)
глицерол (глицерин)
бензойная кислота
натрия сахаринат
натрия гидроксид*
ванилин
ароматизатор** корица
вода очищенная
* - используют натрия гидроксида раствор 30 %.
** - в состав ароматизатора входит 1,2-пропиленгликоль.
6.2 Несовместимость
Не применимо.
6.3 Срок годности (срок хранения)
2 года.
Вскрытый флакон использовать в течение 30 суток.
6.4 Особые меры предосторожности при хранении
Не применять по истечении срока годности, указанного на упаковке.
Хранить при температуре ниже 25 °С.
Условия хранения после первого вскрытия лекарственного препарата см. в разделе 6.3.
6.5 Характер и содержание первичной упаковки
Раствор для приема внутрь, 1,5 мг/мл.
По 100 или 200 мл во флакон из темного стекла 3 гидролитического класса, укупоренный полимерной крышкой из полиэтилена с контролем первого вскрытия или полимерной крышкой из полипропилена с контролем первого вскрытия и защитой от вскрытия детьми.
На флакон наклеивают этикетку самоклеящуюся.
1 флакон вместе с мерной ложкой, с листком-вкладышем помещают в пачку из картона.
6.6 Особые меры предосторожности при уничтожении использованного лекарственного препарата или отходов, полученных после применения лекарственного препарата или работы с ним
Следует промывать и высушивать мерный колпачок после каждого применения. Если препарат применяется несколькими пациентами, то мерный колпачок должен промываться и высушиваться между применением у разных пациентов.
Нет особых требований к утилизации.
7. ДЕРЖАТЕЛЬ РЕГИСТРАЦИОННОГО УДОСТОВЕРЕНИЯ
Россия
Открытое акционерное общество "Фармстандарт-Лексредства" (ОАО "Фармстандарт-Лексредства")
Адрес: 305022, Курская обл., г. Курск, ул. 2-я Агрегатная, д. lа/18
Тел. /факс: (4712) 34-03-13
Электронная почта: leksredstva@pharmstd.ru
7.1 Представитель держателя регистрационного удостоверения
Претензии потребителей направлять по адресу:
Россия
Открытое акционерное общество "Фармстандарт-Лексредства" (ОАО "Фармстандарт-Лексредства")
Адрес: 305022, Курская обл., г. Курск, ул. 2-я Агрегатная, д. 1а/18
Тел. /факс: (4712) 34-03-13
Электронная почта: leksredstva@pharmstd.ru

Телефон: +7 (495) 970 0030
Факс: +7 (495) 970 0032
Московская область,
г. Долгопрудный Лихачевский проезд, дом 5Б
© 2007–